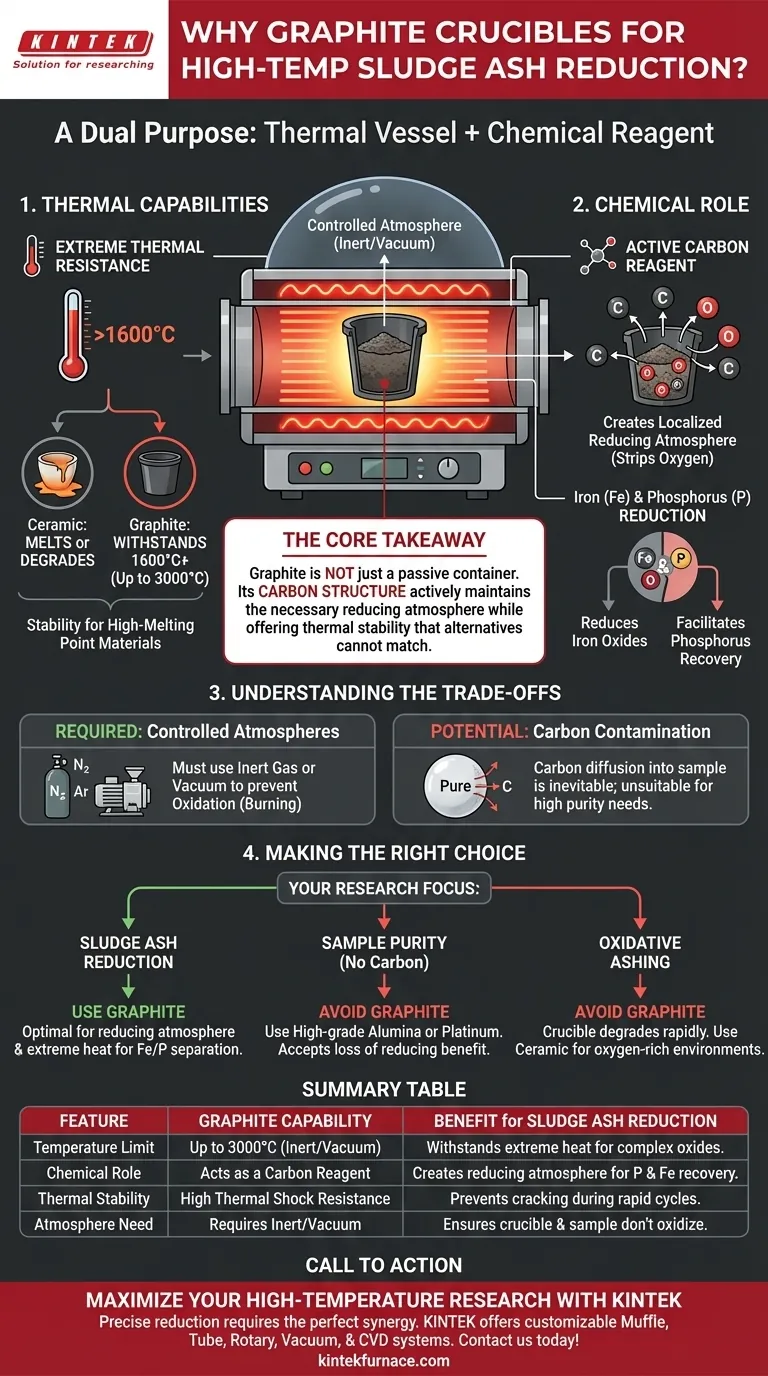
Graphittiegel sind für die Hochtemperatur-Schlammasche-Reduktion unverzichtbar, da sie einen doppelten Zweck erfüllen: Sie dienen sowohl als hochhitzebeständiges Gefäß als auch als aktiver chemischer Teilnehmer am Reduktionsprozess. Indem sie Temperaturen von über 1600 °C standhalten und eine Kohlenstoffquelle bereitstellen, stabilisieren sie die thermische Umgebung und erleichtern gleichzeitig die chemische Umwandlung der Asche.
Die Kernbotschaft Bei der Schlammasche-Reduktion ist der Tiegel nicht nur ein passiver Behälter; er ist ein Reagenz. Graphit wird benötigt, weil seine Kohlenstoffstruktur aktiv die notwendige reduzierende Atmosphäre aufrechterhält, die Trennung von Phosphor und Eisen unterstützt und gleichzeitig eine thermische Stabilität bietet, die Keramik- oder Metallalternativen nicht erreichen können.

Thermische Fähigkeiten in extremen Umgebungen
Widerstandsfähigkeit gegenüber Temperaturen über 1600 °C
Standard-Labor-Keramiken zersetzen sich oder schmelzen oft unter der intensiven Hitze, die für die Asche-Reduktion erforderlich ist. Graphittiegel besitzen eine ausgezeichnete Hitzebeständigkeit und behalten ihre strukturelle Integrität weit über dem Schwellenwert von 1600 °C, der oft für diese Experimente erforderlich ist.
Stabilität für Materialien mit hohem Schmelzpunkt
Schlammasche enthält komplexe Oxide, deren Zersetzung erhebliche Energie erfordert. Graphit ist in der Lage, bei Temperaturen über 2000 °C und sogar bis zu 3000 °C in Vakuumumgebungen stabil zu bleiben. Dies stellt sicher, dass das Gefäß nicht versagt, bevor die Probe vollständig reagiert hat.
Die chemische Rolle: Graphit als Reagenz
Erzeugung einer lokalisierten reduzierenden Atmosphäre
Das bestimmende Merkmal eines Graphittiegels ist, dass er aus Kohlenstoff besteht. Während des Erhitzens weist das Tiegelmaterial selbst reduzierende Eigenschaften auf. Dies erzeugt effektiv eine reduzierende Mikroumgebung um die Probe und entzieht der Schlammasche Sauerstoff.
Erleichterung der Eisen- und Phosphorreduktion
Schlammasche ist häufig reich an Eisen und Phosphor. Die Graphitschnittstelle nimmt an der Reaktion teil und hilft bei der Reduktion von Eisenoxiden. Darüber hinaus sind diese Kohlenstoffkontakte entscheidend für die Schaffung der spezifischen atmosphärischen Bedingungen, die für die erfolgreiche Reduktion von Phosphor notwendig sind, was dessen Rückgewinnung oder Trennung ermöglicht.
Verständnis der Kompromisse
Die Notwendigkeit kontrollierter Atmosphären
Die Affinität von Graphit zu Sauerstoff ist ein zweischneidiges Schwert. Während es die Reduktion unterstützt, oxidiert (verbrennt) der Tiegel selbst, wenn er bei hohen Temperaturen normaler Luft ausgesetzt wird. Daher müssen diese Experimente in einem Rohrofen unter Inertgasatmosphäre (wie Stickstoff oder Argon) oder Vakuum stattfinden, um zu verhindern, dass sich der Tiegel zersetzt.
Potenzial für Kohlenstoffkontamination
Da der Tiegel an der Reaktion teilnimmt, ist die Diffusion von Kohlenstoff in die Probe unvermeidlich. Während dies für Reduktionsversuche erwünscht ist, macht es Graphit ungeeignet für Prozesse, die hochreine Proben erfordern, bei denen die Einführung von Kohlenstoff als Verunreinigung betrachtet würde.
Die richtige Wahl für Ihr Experiment treffen
Wenn Ihr Hauptaugenmerk auf der Schlammasche-Reduktion liegt:
- Verwenden Sie Graphit: Es ist die optimale Wahl, um die notwendige reduzierende Atmosphäre für die Trennung von Eisen und Phosphor zu gewährleisten und gleichzeitig extremer Hitze standzuhalten.
Wenn Ihr Hauptaugenmerk auf der Probenreinheit (kein Kohlenstoff) liegt:
- Vermeiden Sie Graphit: Entscheiden Sie sich für hochwertige Aluminiumoxid- oder Platintiegel und akzeptieren Sie, dass Sie die inhärenten reduzierenden Vorteile des Gefäßes verlieren.
Wenn Ihr Hauptaugenmerk auf der oxidativen Veraschung liegt:
- Vermeiden Sie Graphit: Der Tiegel zersetzt sich schnell; verwenden Sie Keramikgefäße, die für sauerstoffreiche Umgebungen ausgelegt sind.
Graphit ist nicht nur ein Gefäß; es ist eine entscheidende Komponente der chemischen Gleichung, die den Reduktionsprozess zum Abschluss bringt.
Zusammenfassungstabelle:
| Merkmal | Fähigkeit des Graphittiegels | Vorteil für die Schlammasche-Reduktion |
|---|---|---|
| Temperaturgrenze | Bis zu 3000 °C (Inert/Vakuum) | Hält der extremen Hitze stand, die zur Zersetzung komplexer Oxide erforderlich ist. |
| Chemische Rolle | Wirkt als Kohlenstoffreagenz | Erzeugt die reduzierende Atmosphäre, die zur Rückgewinnung von Phosphor und Eisen erforderlich ist. |
| Thermische Stabilität | Hohe Thermoschockbeständigkeit | Verhindert Rissbildung oder Versagen des Gefäßes während schneller Hochtemperaturzyklen. |
| Atmosphärenbedarf | Benötigt Inertgas/Vakuum | Stellt sicher, dass der Tiegel und die Probe nicht vorzeitig oxidieren. |
Maximieren Sie Ihre Hochtemperaturforschung mit KINTEK
Die präzise Reduktion von Schlammasche erfordert die perfekte Synergie zwischen Ihrem Reaktionsgefäß und Ihrem Ofen. KINTEK liefert die Hochleistungsgeräte, die Sie benötigen, um wiederholbare, genaue Ergebnisse zu erzielen. Unterstützt durch erstklassige F&E und Weltklasse-Fertigung bieten wir eine umfassende Palette von Muffel-, Rohr-, Dreh-, Vakuum- und CVD-Systemen, die alle vollständig an Ihre individuellen Laboranforderungen angepasst werden können.
Ob Sie die Phosphorrückgewinnung skalieren oder die Materialreinheit verfeinern, unser Team ist bereit, die thermischen Lösungen zu liefern, die Ihre Forschung erfordert. Kontaktieren Sie KINTEK noch heute, um Ihre kundenspezifischen Ofenanforderungen zu besprechen und zu erfahren, wie unsere Expertise Ihren nächsten Durchbruch vorantreiben kann.
Visuelle Anleitung
Referenzen
- Antoinette Kotzé, Sander Arnout. Thermochemical evaluation of elemental phosphorus recovery from sewage sludge. DOI: 10.17159/2411-9717/3556/2025
Dieser Artikel basiert auch auf technischen Informationen von Kintek Furnace Wissensdatenbank .
Ähnliche Produkte
- 1700 °C Hochtemperatur-Labor-Rohroofen mit Aluminiumoxid-Rohr
- 1400℃ Hochtemperatur-Laborrohrofen mit Aluminiumoxidrohr
- 1400℃ Muffelofen Ofen für Labor
- 1700℃ Hochtemperatur Muffelofen Ofen für Labor
- 1200℃ geteilter Rohrofen Labor-Quarzrohrofen mit Quarzrohr
Andere fragen auch
- Warum ist eine strenge Kontrolle des Vakuumdrucks beim EB-PBF von Ti–6Al–4V unerlässlich? Gewährleistung von Reinheit und Strahlenpräzision
- Welche Funktionen erfüllt Glukose bei der Synthese von Lithium-Ionen-Sieben? Verbesserung der Karbothermischen Reduktion für LiMnO2-Reinheit
- Wie beeinflusst die Wahl der Keramikformen die Ergebnisse bei der Herstellung von Stahlprobenblöcken? Gewährleistung maximaler Probenreinheit
- Was ist der Zweck der Argon-Einblasung von unten? Verbesserung der Sicherheit und Reinigungseffizienz von Lithium-Ionen-Batterien
- Was ist die Funktion der Wassereinspritzung bei der thermischen Holzmodifikation? Überlegene Stabilität und Hydrophobizität freisetzen



















