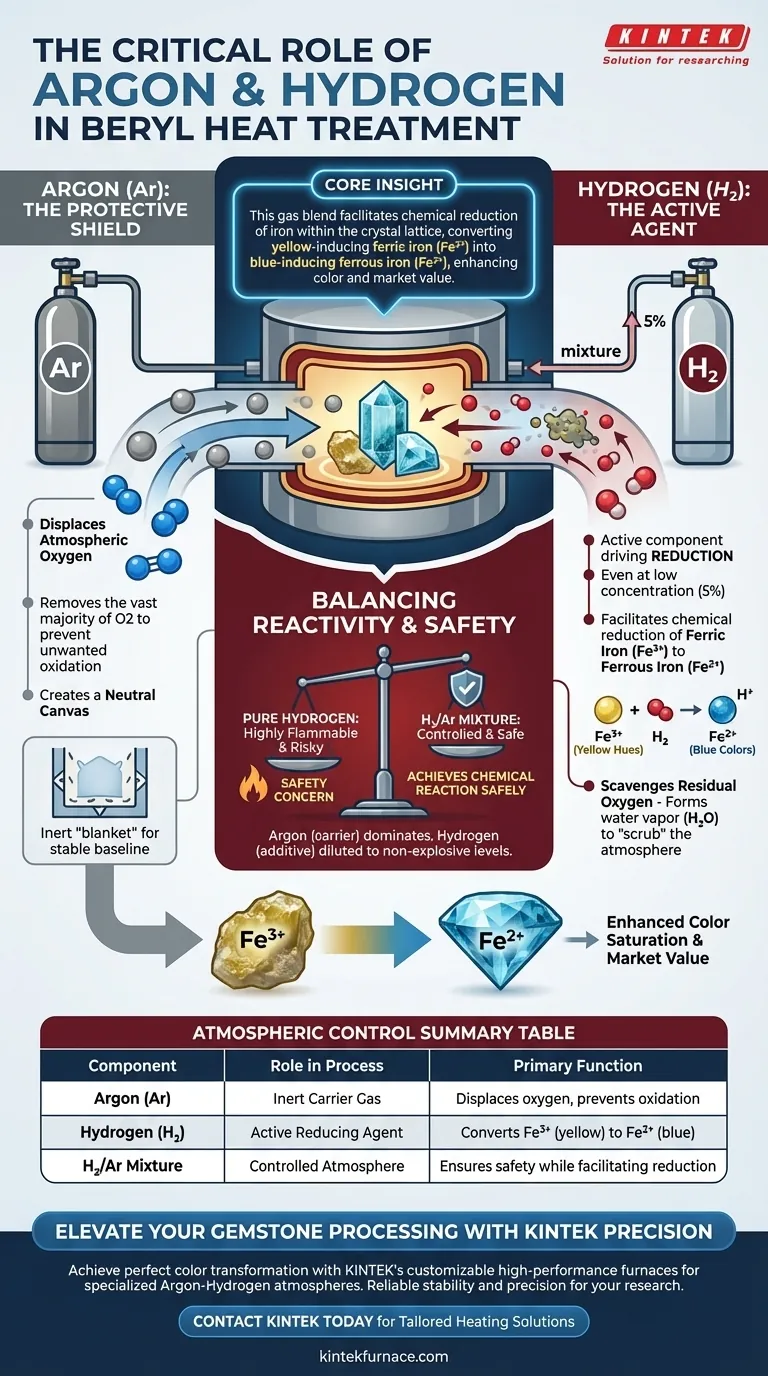
Die Mischung aus Argon (Ar) und Wasserstoff (H2) erfüllt eine kritische Doppelfunktion, die für die Farbveränderung von Beryll-Edelsteinen unerlässlich ist. Argon dient als inerter "Schutzschild", um Luftsauerstoff zu verdrängen, während Wasserstoff als aktives Reduktionsmittel wirkt, das die Verunreinigungen des Steins chemisch verändert. Diese Kombination schafft eine kontrollierte Umgebung, in der Oxidation verhindert und eine günstige Farbtransformation induziert wird.
Kern Erkenntnis Diese Gasmischung ist zwingend erforderlich, um die chemische Reduktion von Eisen im Kristallgitter zu ermöglichen. Durch die Umwandlung von gelb-induzierendem Eisen(III)-oxid ($Fe^{3+}$) in blau-induzierendes Eisen(II)-oxid ($Fe^{2+}$) verbessert die Behandlung permanent die Farbsättigung und den Marktwert des Berylls.

Die Rolle von Argon: Der Schutzschild
Verdrängung von Luftsauerstoff
Argon ist ein inertes Edelgas, was bedeutet, dass es keine chemischen Reaktionen mit dem Edelstein eingeht. Sein Hauptzweck in diesem Prozess ist es, als Schutzvolumen zu fungieren.
Durch das Fluten der Ofenkammer mit Argon wird die Umgebungsluft physikalisch verdrängt. Dies entfernt den Großteil des Sauerstoffs, der notwendig ist, um unerwünschte Oxidation des Edelsteins oder der Ofenkomponenten zu verhindern.
Schaffung einer neutralen Leinwand
Argon schafft eine stabile, neutrale Basis für die Wärmebehandlung. Ohne diese inerte "Decke" würden die später eingeführten reaktiven Gase unvorhersehbar mit atmosphärischen Elementen interagieren.
Die Rolle von Wasserstoff: Das aktive Mittel
Der Reduktionsmechanismus
Wasserstoff ist die aktive Komponente, die das spezifisch gewünschte Ergebnis erzielt: Reduktion. Selbst in geringer Konzentration (typischerweise 5 %) wirkt Wasserstoff als starkes Reduktionsmittel.
Die Wärmebehandlung zielt auf Eisenverunreinigungen im Beryll ab. Wasserstoff erleichtert die chemische Reduktion von Eisen(III)-oxid ($Fe^{3+}$), das gelbe Töne verursacht, zu Eisen(II)-oxid ($Fe^{2+}$).
Verbesserung der Farbsättigung
Diese chemische Verschiebung ist das "Warum" hinter dem Prozess. Die Umwandlung in $Fe^{2+}$ ist für die Erzeugung der begehrten blauen Farben verantwortlich, die oft in Aquamarin und anderen Beryll-Varietäten gesucht werden.
Abfangen von Rest-Sauerstoff
Während Argon den größten Teil der Luft verdrängt, können Spuren von Sauerstoff verbleiben. Wasserstoff reagiert mit diesem Rest-Sauerstoff zu Wasserdampf und "reinigt" so effektiv die Atmosphäre, um eine reine Reduktionsumgebung zu gewährleisten.
Verständnis der Kompromisse
Balance zwischen Reaktivität und Sicherheit
Sie fragen sich vielleicht, warum kein reiner Wasserstoff verwendet wird. Reiner Wasserstoff ist hochentzündlich und birgt erhebliche Sicherheitsrisiken in Hochtemperaturöfen.
Durch die Verwendung einer Mischung, bei der Argon das Hauptträgergas ist und Wasserstoff ein geringer Zusatzstoff (5 %) ist, erzielen Sie die notwendige chemische Reaktion ohne die Flüchtigkeit einer reinen Wasserstoffatmosphäre.
Notwendigkeit der Mischung
Die alleinige Verwendung von Argon würde Oxidation verhindern, aber die Farbe nicht verbessern, da kein Reduktionsmittel vorhanden wäre, um das Eisen umzuwandeln. Umgekehrt würde eine sauerstoffreiche Umgebung die Reduktion gänzlich verhindern. Daher ist die spezifische Mischung für die Farbverbesserung nicht verhandelbar.
Die richtige Wahl für Ihr Ziel treffen
Um die gewünschten ästhetischen Ergebnisse bei der Wärmebehandlung von Beryll zu erzielen, müssen Sie die Atmosphäre basierend auf der spezifischen erforderlichen Eisenumwandlung steuern.
- Wenn Ihr Hauptaugenmerk auf der Eliminierung gelber Töne liegt: Sie müssen Wasserstoff einleiten, um $Fe^{3+}$ Ionen erfolgreich zu $Fe^{2+}$ zu reduzieren.
- Wenn Ihr Hauptaugenmerk auf der Prozesssicherheit liegt: Verlassen Sie sich auf Argon als Hauptträgergas, um einen positiven Druck aufrechtzuerhalten und den brennbaren Wasserstoff auf nicht-explosive Mengen zu verdünnen.
Präzise Atmosphärenkontrolle ist der einzige Weg, um die begehrten blauen Töne, die in der Struktur des Edelsteins verborgen sind, zuverlässig freizusetzen.
Zusammenfassungstabelle:
| Komponente | Rolle im Prozess | Hauptfunktion |
|---|---|---|
| Argon (Ar) | Inertes Trägergas | Verdrängt Sauerstoff und verhindert unerwünschte Oxidation |
| Wasserstoff (H2) | Aktives Reduktionsmittel | Wandelt $Fe^{3+}$ (gelb) in $Fe^{2+}$ (blau) um |
| H2/Ar-Mischung | Kontrollierte Atmosphäre | Gewährleistet Sicherheit bei gleichzeitiger Ermöglichung der chemischen Reduktion |
Verbessern Sie Ihre Edelsteinverarbeitung mit KINTEK Präzision
Die perfekte Farbtransformation bei Beryll erfordert absolute Kontrolle über Ihre thermische Umgebung. Gestützt auf F&E und Fertigungsexpertise bietet KINTEK Hochleistungs-Muffel-, Rohr-, Rotations-, Vakuum- und CVD-Systeme – alle vollständig anpassbar für die Handhabung spezialisierter Argon-Wasserstoff-Atmosphären.
Ob Sie gelbe Töne eliminieren oder die Prozesssicherheit maximieren möchten, unsere Labor-Hochtemperaturöfen bieten die Stabilität und Präzision, die Ihre Forschung erfordert. Kontaktieren Sie KINTEK noch heute, um zu erfahren, wie unsere maßgeschneiderten Heizlösungen die Effizienz und den Output Ihres Labors verbessern können.
Visuelle Anleitung
Referenzen
- Bin Hao, Qingfeng Guo. The Effect of Heat Treatment on Yellow-Green Beryl Color and Its Enhancement Mechanism. DOI: 10.3390/cryst15080746
Dieser Artikel basiert auch auf technischen Informationen von Kintek Furnace Wissensdatenbank .
Ähnliche Produkte
- Mesh Belt Ofen mit kontrollierter Atmosphäre Ofen mit inerter Stickstoffatmosphäre
- 1400℃ Gesteuerter Ofen mit inerter Stickstoffatmosphäre
- 1200℃ Schutzgasofen mit kontrollierter Stickstoffatmosphäre
- Vakuum-Wärmebehandlungsofen zum Sintern und Löten
- 1700℃ Gesteuerter Ofen mit inerter Stickstoffatmosphäre
Andere fragen auch
- Was sind die zwei Hauptzwecke von Schutzgasatmosphären in Öfen? Materialien schützen oder umwandeln für Spitzenleistung
- Wie gewährleistet ein Ofen mit kontrollierter Atmosphäre Präzision und Zuverlässigkeit? Erzielen Sie eine konsistente Materialverarbeitung
- Wie wird ein Ofen mit kontrollierter Atmosphäre in der Materialforschung eingesetzt? Präzise Materialsynthese und -wärmebehandlung erreichen
- Welche Arten von Öfen haben kontrollierte Atmosphärenöfen größtenteils ersetzt? Steigern Sie die metallurgische Präzision und Sicherheit
- Welche Arten von Gasen kann ein Schutzgasofen handhaben? Beherrschen Sie Inert- und Reaktivgase für Ihr Labor















